QUÍMICA ORGÂNICA II
Quando um nucleófilo ataca o carbono carbonílico, a ligação pi carbono-oxigênio quebra e um intermediário é formado. O intermediário é chamado intermediário tetraédrico porque o carbono trigonal sp2 nos reagentes se torna um carbono tetraédrico sp3. Com relação ao mecanismo representado abaixo, assinale a alternativa correta.
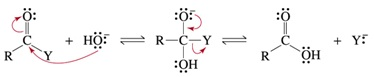
O grupo Y foi eliminado pelo fato de formar uma base mais fraca que o grupo OH.
Quanto mais forte for a base melhor será como grupo de saída.
Se os grupos OH- e Y- tiverem basicidade similares a reação não ocorre.
A entrada do grupo OH- indica que a reação é uma substituição eletrofílica.
No intermediário tetraédrico é mais fácil ocorrer a eliminação do grupo OH.
A reatividade das substâncias carboniladas está relacionada com a polaridade do grupo carbonila. O oxigênio é mais eletronegativo do que o carbono. O carbono carbonílico, portanto, é um eletrófilo e por esse motivo está susceptível ao ataque de um nucleófilo. Com relação aos dois sentidos da reação, pode-se afirmar que:
Dados: MeOH (pKa = 16) ; NH3 (pKa = 9,25)
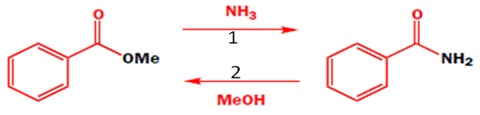
A reação pode ocorrer nos dois sentidos, mas preferencialmente no sentido 2.
A reação no sentido 1 não ocorre, porque o NH3 é um nucleófilo fraco.
O grupo NH2- é uma base mais fraca que o grupo MeO-.
A reação no sentido 1 ocorre, pelo fato do grupo OMe ser um melhor grupo de saída.
A reação no sentido 2 ocorre e o grupo NH2- será eliminado no intermediário da reação.
A palavra nucleófilo em química é designada a uma espécie (átomo ou molécula) rica em elétrons. Já a palavra eletrófilo significa "gostar de elétrons". É possível conceituar um eletrófilo como sendo uma espécie (átomo ou molécula) deficiente de elétrons. Das espécies químicas mencionadas abaixo, em qual das alternativas é possível encontrar um eletrófilo e um nucleófilo, respectivamente:
CH3CH2+ e H+
Cl- e H2O
OH- e H+
H+ e BH3
CH3CH2+ e H2O
Considere as substâncias fenol, ácido acético, ácido benzóico e cloreto de metilamônio. Em relação a essas substâncias e a suas soluções aquosas de mesma concentração em mol.L-1, todas as alternativas estão corretas, EXCETO.
O pH da solução de fenol é maior do que o da solução de ácido acético.
A solução de cloreto de metilamônio tem pH menor do que sete.
O fenol é uma base segundo a teoria de Arrhenius.
O ácido benzóico é um composto aromático.
O ácido acético reage com carbonatos produzindo gás carbônico.
Considerando a teoria de Bronsted-Lowry, ácido é toda espécie capaz de doar próton (H+) e base é toda espécie química capaz de receber próton (H+). Na reação a seguir:
NH3 + H2O ↔ NH4+ + OH- Quais espécies podem ser consideradas bases de Bronsted-Lowry?
NH3 e NH4+
NH3 e H3O+
NH3 e OH
H3O+ e OH
H2O e NH4+
Os ácidos orgânicos e os fenóis possuem caráter ácido, ou seja, ionizam liberando íons H+ quando em solução aquosa. Mas quando comparados aos ácidos inorgânicos, são bem mais fracos. No entanto, a presença de determinados grupos ligados ao átomo de carbono, provoca um aumento na ionização do composto. Considere uma substância representada pela estrutura abaixo:
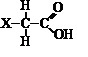 A substância acima estará mais ionizada em solução aquosa se X representar o grupo substituinte:
A substância acima estará mais ionizada em solução aquosa se X representar o grupo substituinte:
CH2CH3
CH3
F
I
H
Em toda reação química é necessário que aconteça a quebra de uma ligação para formação de outra substância. Essa quebra pode acontecer de duas formas: cisão homolítica e heterolítica. Sobre essas duas formas de quebra de ligação, marque a alternativa correta.
A cisão homolítica é mais comum de acontecer que a cisão heterolítica.
Na cisão heterolítica, o par de elétrons da ligação é dividido entre os átomos que compõe a ligação.
Na cisão heterolítica, o par de elétrons da ligação ficará com apenas uma das espécies.
Na cisão homolítica, o par de elétrons da ligação ficará com apenas um átomo que compõe a ligação.
Na cisão heterolítica, pode ocorrer a formação de espécies radicalares.
Os valores Ka e pKa indicam a força ácida de um determinado composto. Quanto menor o valor de pKa, maior será seu valor de Ka e consequentemente maior é a força ácida da substância. Considere a tabela a seguir, que apresenta os valores de pKa e da temperatura de ebulição de três compostos.

Os compostos A, B e C podem ser, respectivamente:
etanol - fenol - ácido acético.
ácido acético - etanol - fenol.
ácido acético - fenol - etanol.
fenol - etanol - ácido acético.
fenol - ácido acético - etanol.
Os ácidos carboxílicos e os fenóis, devido ao seu caráter ácido, quando reagem com bases inorgânicas levam à formação de seus respectivos sais orgânicos. Sendo assim, quando ocorrer a reação do ácido pentanóico com o hidróxido de lítio, qual será o sal formado?
Pentanoato de lítio.
Etanoato de potássio.
Propanoato de Lítio.
Hexanoato de Lítio.
Pentanoato de sódio.
A metilamina é um produto gasoso formado na decomposição da carne de peixe, responsável pelo odor característico que impregna as mãos de quem trabalha com peixe. A prática mostra que é mais fácil remover o odor de peixe das mãos esfregando-as primeiro com suco de limão ou vinagre, e depois lavando com água pura, do que diretamente com água e sabão. Com base nestas informações, considere o seguinte texto sobre a metilamina:
A metilamina é um gás bastante solúvel em água. Tem propriedades..............., por conter na molécula o grupo amina. Reage com ................, produzindo o sal CH3NH3+Cl-. Esse sal, quando puro e dissolvido em água, por hidrólise, forma uma solução de caráter....................
O texto é completado de forma correta, respectivamente, por:
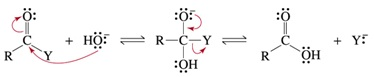
O grupo Y foi eliminado pelo fato de formar uma base mais fraca que o grupo OH.
Quanto mais forte for a base melhor será como grupo de saída.
Se os grupos OH- e Y- tiverem basicidade similares a reação não ocorre.
A entrada do grupo OH- indica que a reação é uma substituição eletrofílica.
No intermediário tetraédrico é mais fácil ocorrer a eliminação do grupo OH.
A reatividade das substâncias carboniladas está relacionada com a polaridade do grupo carbonila. O oxigênio é mais eletronegativo do que o carbono. O carbono carbonílico, portanto, é um eletrófilo e por esse motivo está susceptível ao ataque de um nucleófilo. Com relação aos dois sentidos da reação, pode-se afirmar que:
Dados: MeOH (pKa = 16) ; NH3 (pKa = 9,25)

A reação pode ocorrer nos dois sentidos, mas preferencialmente no sentido 2.
A reação no sentido 1 não ocorre, porque o NH3 é um nucleófilo fraco.
O grupo NH2- é uma base mais fraca que o grupo MeO-.
A reação no sentido 1 ocorre, pelo fato do grupo OMe ser um melhor grupo de saída.
A reação no sentido 2 ocorre e o grupo NH2- será eliminado no intermediário da reação.
A palavra nucleófilo em química é designada a uma espécie (átomo ou molécula) rica em elétrons. Já a palavra eletrófilo significa "gostar de elétrons". É possível conceituar um eletrófilo como sendo uma espécie (átomo ou molécula) deficiente de elétrons. Das espécies químicas mencionadas abaixo, em qual das alternativas é possível encontrar um eletrófilo e um nucleófilo, respectivamente:
CH3CH2+ e H+
Cl- e H2O
OH- e H+
H+ e BH3
CH3CH2+ e H2O
Considere as substâncias fenol, ácido acético, ácido benzóico e cloreto de metilamônio. Em relação a essas substâncias e a suas soluções aquosas de mesma concentração em mol.L-1, todas as alternativas estão corretas, EXCETO.
O pH da solução de fenol é maior do que o da solução de ácido acético.
A solução de cloreto de metilamônio tem pH menor do que sete.
O fenol é uma base segundo a teoria de Arrhenius.
O ácido benzóico é um composto aromático.
O ácido acético reage com carbonatos produzindo gás carbônico.
Considerando a teoria de Bronsted-Lowry, ácido é toda espécie capaz de doar próton (H+) e base é toda espécie química capaz de receber próton (H+). Na reação a seguir:
NH3 + H2O ↔ NH4+ + OH- Quais espécies podem ser consideradas bases de Bronsted-Lowry?
NH3 e NH4+
NH3 e H3O+
NH3 e OH
H3O+ e OH
H2O e NH4+
Os ácidos orgânicos e os fenóis possuem caráter ácido, ou seja, ionizam liberando íons H+ quando em solução aquosa. Mas quando comparados aos ácidos inorgânicos, são bem mais fracos. No entanto, a presença de determinados grupos ligados ao átomo de carbono, provoca um aumento na ionização do composto. Considere uma substância representada pela estrutura abaixo:
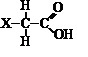 A substância acima estará mais ionizada em solução aquosa se X representar o grupo substituinte:
A substância acima estará mais ionizada em solução aquosa se X representar o grupo substituinte:
CH2CH3
CH3
F
I
H
Em toda reação química é necessário que aconteça a quebra de uma ligação para formação de outra substância. Essa quebra pode acontecer de duas formas: cisão homolítica e heterolítica. Sobre essas duas formas de quebra de ligação, marque a alternativa correta.
A cisão homolítica é mais comum de acontecer que a cisão heterolítica.
Na cisão heterolítica, o par de elétrons da ligação é dividido entre os átomos que compõe a ligação.
Na cisão heterolítica, o par de elétrons da ligação ficará com apenas uma das espécies.
Na cisão homolítica, o par de elétrons da ligação ficará com apenas um átomo que compõe a ligação.
Na cisão heterolítica, pode ocorrer a formação de espécies radicalares.
Os valores Ka e pKa indicam a força ácida de um determinado composto. Quanto menor o valor de pKa, maior será seu valor de Ka e consequentemente maior é a força ácida da substância. Considere a tabela a seguir, que apresenta os valores de pKa e da temperatura de ebulição de três compostos.

Os compostos A, B e C podem ser, respectivamente:
etanol - fenol - ácido acético.
ácido acético - etanol - fenol.
ácido acético - fenol - etanol.
fenol - etanol - ácido acético.
fenol - ácido acético - etanol.
Os ácidos carboxílicos e os fenóis, devido ao seu caráter ácido, quando reagem com bases inorgânicas levam à formação de seus respectivos sais orgânicos. Sendo assim, quando ocorrer a reação do ácido pentanóico com o hidróxido de lítio, qual será o sal formado?
Pentanoato de lítio.
Etanoato de potássio.
Propanoato de Lítio.
Hexanoato de Lítio.
Pentanoato de sódio.
A metilamina é um produto gasoso formado na decomposição da carne de peixe, responsável pelo odor característico que impregna as mãos de quem trabalha com peixe. A prática mostra que é mais fácil remover o odor de peixe das mãos esfregando-as primeiro com suco de limão ou vinagre, e depois lavando com água pura, do que diretamente com água e sabão. Com base nestas informações, considere o seguinte texto sobre a metilamina:
A metilamina é um gás bastante solúvel em água. Tem propriedades..............., por conter na molécula o grupo amina. Reage com ................, produzindo o sal CH3NH3+Cl-. Esse sal, quando puro e dissolvido em água, por hidrólise, forma uma solução de caráter....................
O texto é completado de forma correta, respectivamente, por:

A reação pode ocorrer nos dois sentidos, mas preferencialmente no sentido 2.
A reação no sentido 1 não ocorre, porque o NH3 é um nucleófilo fraco.
O grupo NH2- é uma base mais fraca que o grupo MeO-.
A reação no sentido 1 ocorre, pelo fato do grupo OMe ser um melhor grupo de saída.
A reação no sentido 2 ocorre e o grupo NH2- será eliminado no intermediário da reação.
A palavra nucleófilo em química é designada a uma espécie (átomo ou molécula) rica em elétrons. Já a palavra eletrófilo significa "gostar de elétrons". É possível conceituar um eletrófilo como sendo uma espécie (átomo ou molécula) deficiente de elétrons. Das espécies químicas mencionadas abaixo, em qual das alternativas é possível encontrar um eletrófilo e um nucleófilo, respectivamente:
CH3CH2+ e H+
Cl- e H2O
OH- e H+
H+ e BH3
CH3CH2+ e H2O
Considere as substâncias fenol, ácido acético, ácido benzóico e cloreto de metilamônio. Em relação a essas substâncias e a suas soluções aquosas de mesma concentração em mol.L-1, todas as alternativas estão corretas, EXCETO.
O pH da solução de fenol é maior do que o da solução de ácido acético.
A solução de cloreto de metilamônio tem pH menor do que sete.
O fenol é uma base segundo a teoria de Arrhenius.
O ácido benzóico é um composto aromático.
O ácido acético reage com carbonatos produzindo gás carbônico.
Considerando a teoria de Bronsted-Lowry, ácido é toda espécie capaz de doar próton (H+) e base é toda espécie química capaz de receber próton (H+). Na reação a seguir:
NH3 + H2O ↔ NH4+ + OH- Quais espécies podem ser consideradas bases de Bronsted-Lowry?
NH3 e NH4+
NH3 e H3O+
NH3 e OH
H3O+ e OH
H2O e NH4+
Os ácidos orgânicos e os fenóis possuem caráter ácido, ou seja, ionizam liberando íons H+ quando em solução aquosa. Mas quando comparados aos ácidos inorgânicos, são bem mais fracos. No entanto, a presença de determinados grupos ligados ao átomo de carbono, provoca um aumento na ionização do composto. Considere uma substância representada pela estrutura abaixo:
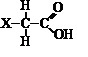 A substância acima estará mais ionizada em solução aquosa se X representar o grupo substituinte:
A substância acima estará mais ionizada em solução aquosa se X representar o grupo substituinte:
CH2CH3
CH3
F
I
H
Em toda reação química é necessário que aconteça a quebra de uma ligação para formação de outra substância. Essa quebra pode acontecer de duas formas: cisão homolítica e heterolítica. Sobre essas duas formas de quebra de ligação, marque a alternativa correta.
A cisão homolítica é mais comum de acontecer que a cisão heterolítica.
Na cisão heterolítica, o par de elétrons da ligação é dividido entre os átomos que compõe a ligação.
Na cisão heterolítica, o par de elétrons da ligação ficará com apenas uma das espécies.
Na cisão homolítica, o par de elétrons da ligação ficará com apenas um átomo que compõe a ligação.
Na cisão heterolítica, pode ocorrer a formação de espécies radicalares.
Os valores Ka e pKa indicam a força ácida de um determinado composto. Quanto menor o valor de pKa, maior será seu valor de Ka e consequentemente maior é a força ácida da substância. Considere a tabela a seguir, que apresenta os valores de pKa e da temperatura de ebulição de três compostos.

Os compostos A, B e C podem ser, respectivamente:
etanol - fenol - ácido acético.
ácido acético - etanol - fenol.
ácido acético - fenol - etanol.
fenol - etanol - ácido acético.
fenol - ácido acético - etanol.
Os ácidos carboxílicos e os fenóis, devido ao seu caráter ácido, quando reagem com bases inorgânicas levam à formação de seus respectivos sais orgânicos. Sendo assim, quando ocorrer a reação do ácido pentanóico com o hidróxido de lítio, qual será o sal formado?
Pentanoato de lítio.
Etanoato de potássio.
Propanoato de Lítio.
Hexanoato de Lítio.
Pentanoato de sódio.
A metilamina é um produto gasoso formado na decomposição da carne de peixe, responsável pelo odor característico que impregna as mãos de quem trabalha com peixe. A prática mostra que é mais fácil remover o odor de peixe das mãos esfregando-as primeiro com suco de limão ou vinagre, e depois lavando com água pura, do que diretamente com água e sabão. Com base nestas informações, considere o seguinte texto sobre a metilamina:
A metilamina é um gás bastante solúvel em água. Tem propriedades..............., por conter na molécula o grupo amina. Reage com ................, produzindo o sal CH3NH3+Cl-. Esse sal, quando puro e dissolvido em água, por hidrólise, forma uma solução de caráter....................
O texto é completado de forma correta, respectivamente, por:
CH3CH2+ e H+
Cl- e H2O
OH- e H+
H+ e BH3
CH3CH2+ e H2O
Considere as substâncias fenol, ácido acético, ácido benzóico e cloreto de metilamônio. Em relação a essas substâncias e a suas soluções aquosas de mesma concentração em mol.L-1, todas as alternativas estão corretas, EXCETO.
O pH da solução de fenol é maior do que o da solução de ácido acético.
A solução de cloreto de metilamônio tem pH menor do que sete.
O fenol é uma base segundo a teoria de Arrhenius.
O ácido benzóico é um composto aromático.
O ácido acético reage com carbonatos produzindo gás carbônico.
Considerando a teoria de Bronsted-Lowry, ácido é toda espécie capaz de doar próton (H+) e base é toda espécie química capaz de receber próton (H+). Na reação a seguir:
NH3 + H2O ↔ NH4+ + OH- Quais espécies podem ser consideradas bases de Bronsted-Lowry?
NH3 e NH4+
NH3 e H3O+
NH3 e OH
H3O+ e OH
H2O e NH4+
Os ácidos orgânicos e os fenóis possuem caráter ácido, ou seja, ionizam liberando íons H+ quando em solução aquosa. Mas quando comparados aos ácidos inorgânicos, são bem mais fracos. No entanto, a presença de determinados grupos ligados ao átomo de carbono, provoca um aumento na ionização do composto. Considere uma substância representada pela estrutura abaixo:
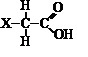 A substância acima estará mais ionizada em solução aquosa se X representar o grupo substituinte:
A substância acima estará mais ionizada em solução aquosa se X representar o grupo substituinte:
CH2CH3
CH3
F
I
H
Em toda reação química é necessário que aconteça a quebra de uma ligação para formação de outra substância. Essa quebra pode acontecer de duas formas: cisão homolítica e heterolítica. Sobre essas duas formas de quebra de ligação, marque a alternativa correta.
A cisão homolítica é mais comum de acontecer que a cisão heterolítica.
Na cisão heterolítica, o par de elétrons da ligação é dividido entre os átomos que compõe a ligação.
Na cisão heterolítica, o par de elétrons da ligação ficará com apenas uma das espécies.
Na cisão homolítica, o par de elétrons da ligação ficará com apenas um átomo que compõe a ligação.
Na cisão heterolítica, pode ocorrer a formação de espécies radicalares.
Os valores Ka e pKa indicam a força ácida de um determinado composto. Quanto menor o valor de pKa, maior será seu valor de Ka e consequentemente maior é a força ácida da substância. Considere a tabela a seguir, que apresenta os valores de pKa e da temperatura de ebulição de três compostos.

Os compostos A, B e C podem ser, respectivamente:
etanol - fenol - ácido acético.
ácido acético - etanol - fenol.
ácido acético - fenol - etanol.
fenol - etanol - ácido acético.
fenol - ácido acético - etanol.
Os ácidos carboxílicos e os fenóis, devido ao seu caráter ácido, quando reagem com bases inorgânicas levam à formação de seus respectivos sais orgânicos. Sendo assim, quando ocorrer a reação do ácido pentanóico com o hidróxido de lítio, qual será o sal formado?
Pentanoato de lítio.
Etanoato de potássio.
Propanoato de Lítio.
Hexanoato de Lítio.
Pentanoato de sódio.
A metilamina é um produto gasoso formado na decomposição da carne de peixe, responsável pelo odor característico que impregna as mãos de quem trabalha com peixe. A prática mostra que é mais fácil remover o odor de peixe das mãos esfregando-as primeiro com suco de limão ou vinagre, e depois lavando com água pura, do que diretamente com água e sabão. Com base nestas informações, considere o seguinte texto sobre a metilamina:
A metilamina é um gás bastante solúvel em água. Tem propriedades..............., por conter na molécula o grupo amina. Reage com ................, produzindo o sal CH3NH3+Cl-. Esse sal, quando puro e dissolvido em água, por hidrólise, forma uma solução de caráter....................
O texto é completado de forma correta, respectivamente, por:
O pH da solução de fenol é maior do que o da solução de ácido acético.
A solução de cloreto de metilamônio tem pH menor do que sete.
O fenol é uma base segundo a teoria de Arrhenius.
O ácido benzóico é um composto aromático.
O ácido acético reage com carbonatos produzindo gás carbônico.
Considerando a teoria de Bronsted-Lowry, ácido é toda espécie capaz de doar próton (H+) e base é toda espécie química capaz de receber próton (H+). Na reação a seguir:
NH3 + H2O ↔ NH4+ + OH- Quais espécies podem ser consideradas bases de Bronsted-Lowry?
NH3 e NH4+
NH3 e H3O+
NH3 e OH
H3O+ e OH
H2O e NH4+
Os ácidos orgânicos e os fenóis possuem caráter ácido, ou seja, ionizam liberando íons H+ quando em solução aquosa. Mas quando comparados aos ácidos inorgânicos, são bem mais fracos. No entanto, a presença de determinados grupos ligados ao átomo de carbono, provoca um aumento na ionização do composto. Considere uma substância representada pela estrutura abaixo:
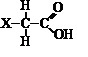 A substância acima estará mais ionizada em solução aquosa se X representar o grupo substituinte:
A substância acima estará mais ionizada em solução aquosa se X representar o grupo substituinte:
CH2CH3
CH3
F
I
H
Em toda reação química é necessário que aconteça a quebra de uma ligação para formação de outra substância. Essa quebra pode acontecer de duas formas: cisão homolítica e heterolítica. Sobre essas duas formas de quebra de ligação, marque a alternativa correta.
A cisão homolítica é mais comum de acontecer que a cisão heterolítica.
Na cisão heterolítica, o par de elétrons da ligação é dividido entre os átomos que compõe a ligação.
Na cisão heterolítica, o par de elétrons da ligação ficará com apenas uma das espécies.
Na cisão homolítica, o par de elétrons da ligação ficará com apenas um átomo que compõe a ligação.
Na cisão heterolítica, pode ocorrer a formação de espécies radicalares.
Os valores Ka e pKa indicam a força ácida de um determinado composto. Quanto menor o valor de pKa, maior será seu valor de Ka e consequentemente maior é a força ácida da substância. Considere a tabela a seguir, que apresenta os valores de pKa e da temperatura de ebulição de três compostos.

Os compostos A, B e C podem ser, respectivamente:
etanol - fenol - ácido acético.
ácido acético - etanol - fenol.
ácido acético - fenol - etanol.
fenol - etanol - ácido acético.
fenol - ácido acético - etanol.
Os ácidos carboxílicos e os fenóis, devido ao seu caráter ácido, quando reagem com bases inorgânicas levam à formação de seus respectivos sais orgânicos. Sendo assim, quando ocorrer a reação do ácido pentanóico com o hidróxido de lítio, qual será o sal formado?
Pentanoato de lítio.
Etanoato de potássio.
Propanoato de Lítio.
Hexanoato de Lítio.
Pentanoato de sódio.
A metilamina é um produto gasoso formado na decomposição da carne de peixe, responsável pelo odor característico que impregna as mãos de quem trabalha com peixe. A prática mostra que é mais fácil remover o odor de peixe das mãos esfregando-as primeiro com suco de limão ou vinagre, e depois lavando com água pura, do que diretamente com água e sabão. Com base nestas informações, considere o seguinte texto sobre a metilamina:
A metilamina é um gás bastante solúvel em água. Tem propriedades..............., por conter na molécula o grupo amina. Reage com ................, produzindo o sal CH3NH3+Cl-. Esse sal, quando puro e dissolvido em água, por hidrólise, forma uma solução de caráter....................
O texto é completado de forma correta, respectivamente, por:
NH3 e NH4+
NH3 e H3O+
NH3 e OH
H3O+ e OH
H2O e NH4+
Os ácidos orgânicos e os fenóis possuem caráter ácido, ou seja, ionizam liberando íons H+ quando em solução aquosa. Mas quando comparados aos ácidos inorgânicos, são bem mais fracos. No entanto, a presença de determinados grupos ligados ao átomo de carbono, provoca um aumento na ionização do composto. Considere uma substância representada pela estrutura abaixo:
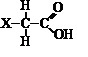 A substância acima estará mais ionizada em solução aquosa se X representar o grupo substituinte:
A substância acima estará mais ionizada em solução aquosa se X representar o grupo substituinte:
CH2CH3
CH3
F
I
H
Em toda reação química é necessário que aconteça a quebra de uma ligação para formação de outra substância. Essa quebra pode acontecer de duas formas: cisão homolítica e heterolítica. Sobre essas duas formas de quebra de ligação, marque a alternativa correta.
A cisão homolítica é mais comum de acontecer que a cisão heterolítica.
Na cisão heterolítica, o par de elétrons da ligação é dividido entre os átomos que compõe a ligação.
Na cisão heterolítica, o par de elétrons da ligação ficará com apenas uma das espécies.
Na cisão homolítica, o par de elétrons da ligação ficará com apenas um átomo que compõe a ligação.
Na cisão heterolítica, pode ocorrer a formação de espécies radicalares.
Os valores Ka e pKa indicam a força ácida de um determinado composto. Quanto menor o valor de pKa, maior será seu valor de Ka e consequentemente maior é a força ácida da substância. Considere a tabela a seguir, que apresenta os valores de pKa e da temperatura de ebulição de três compostos.

Os compostos A, B e C podem ser, respectivamente:
etanol - fenol - ácido acético.
ácido acético - etanol - fenol.
ácido acético - fenol - etanol.
fenol - etanol - ácido acético.
fenol - ácido acético - etanol.
Os ácidos carboxílicos e os fenóis, devido ao seu caráter ácido, quando reagem com bases inorgânicas levam à formação de seus respectivos sais orgânicos. Sendo assim, quando ocorrer a reação do ácido pentanóico com o hidróxido de lítio, qual será o sal formado?
Pentanoato de lítio.
Etanoato de potássio.
Propanoato de Lítio.
Hexanoato de Lítio.
Pentanoato de sódio.
A metilamina é um produto gasoso formado na decomposição da carne de peixe, responsável pelo odor característico que impregna as mãos de quem trabalha com peixe. A prática mostra que é mais fácil remover o odor de peixe das mãos esfregando-as primeiro com suco de limão ou vinagre, e depois lavando com água pura, do que diretamente com água e sabão. Com base nestas informações, considere o seguinte texto sobre a metilamina:
A metilamina é um gás bastante solúvel em água. Tem propriedades..............., por conter na molécula o grupo amina. Reage com ................, produzindo o sal CH3NH3+Cl-. Esse sal, quando puro e dissolvido em água, por hidrólise, forma uma solução de caráter....................
O texto é completado de forma correta, respectivamente, por:
CH2CH3
CH3
F
I
H
Em toda reação química é necessário que aconteça a quebra de uma ligação para formação de outra substância. Essa quebra pode acontecer de duas formas: cisão homolítica e heterolítica. Sobre essas duas formas de quebra de ligação, marque a alternativa correta.
A cisão homolítica é mais comum de acontecer que a cisão heterolítica.
Na cisão heterolítica, o par de elétrons da ligação é dividido entre os átomos que compõe a ligação.
Na cisão heterolítica, o par de elétrons da ligação ficará com apenas uma das espécies.
Na cisão homolítica, o par de elétrons da ligação ficará com apenas um átomo que compõe a ligação.
Na cisão heterolítica, pode ocorrer a formação de espécies radicalares.
Os valores Ka e pKa indicam a força ácida de um determinado composto. Quanto menor o valor de pKa, maior será seu valor de Ka e consequentemente maior é a força ácida da substância. Considere a tabela a seguir, que apresenta os valores de pKa e da temperatura de ebulição de três compostos.

Os compostos A, B e C podem ser, respectivamente:
etanol - fenol - ácido acético.
ácido acético - etanol - fenol.
ácido acético - fenol - etanol.
fenol - etanol - ácido acético.
fenol - ácido acético - etanol.
Os ácidos carboxílicos e os fenóis, devido ao seu caráter ácido, quando reagem com bases inorgânicas levam à formação de seus respectivos sais orgânicos. Sendo assim, quando ocorrer a reação do ácido pentanóico com o hidróxido de lítio, qual será o sal formado?
Pentanoato de lítio.
Etanoato de potássio.
Propanoato de Lítio.
Hexanoato de Lítio.
Pentanoato de sódio.
A metilamina é um produto gasoso formado na decomposição da carne de peixe, responsável pelo odor característico que impregna as mãos de quem trabalha com peixe. A prática mostra que é mais fácil remover o odor de peixe das mãos esfregando-as primeiro com suco de limão ou vinagre, e depois lavando com água pura, do que diretamente com água e sabão. Com base nestas informações, considere o seguinte texto sobre a metilamina:
A metilamina é um gás bastante solúvel em água. Tem propriedades..............., por conter na molécula o grupo amina. Reage com ................, produzindo o sal CH3NH3+Cl-. Esse sal, quando puro e dissolvido em água, por hidrólise, forma uma solução de caráter....................
O texto é completado de forma correta, respectivamente, por:
A cisão homolítica é mais comum de acontecer que a cisão heterolítica.
Na cisão heterolítica, o par de elétrons da ligação é dividido entre os átomos que compõe a ligação.
Na cisão heterolítica, o par de elétrons da ligação ficará com apenas uma das espécies.
Na cisão homolítica, o par de elétrons da ligação ficará com apenas um átomo que compõe a ligação.
Na cisão heterolítica, pode ocorrer a formação de espécies radicalares.
Os valores Ka e pKa indicam a força ácida de um determinado composto. Quanto menor o valor de pKa, maior será seu valor de Ka e consequentemente maior é a força ácida da substância. Considere a tabela a seguir, que apresenta os valores de pKa e da temperatura de ebulição de três compostos.

Os compostos A, B e C podem ser, respectivamente:
etanol - fenol - ácido acético.
ácido acético - etanol - fenol.
ácido acético - fenol - etanol.
fenol - etanol - ácido acético.
fenol - ácido acético - etanol.
Os ácidos carboxílicos e os fenóis, devido ao seu caráter ácido, quando reagem com bases inorgânicas levam à formação de seus respectivos sais orgânicos. Sendo assim, quando ocorrer a reação do ácido pentanóico com o hidróxido de lítio, qual será o sal formado?
Pentanoato de lítio.
Etanoato de potássio.
Propanoato de Lítio.
Hexanoato de Lítio.
Pentanoato de sódio.
A metilamina é um produto gasoso formado na decomposição da carne de peixe, responsável pelo odor característico que impregna as mãos de quem trabalha com peixe. A prática mostra que é mais fácil remover o odor de peixe das mãos esfregando-as primeiro com suco de limão ou vinagre, e depois lavando com água pura, do que diretamente com água e sabão. Com base nestas informações, considere o seguinte texto sobre a metilamina:
A metilamina é um gás bastante solúvel em água. Tem propriedades..............., por conter na molécula o grupo amina. Reage com ................, produzindo o sal CH3NH3+Cl-. Esse sal, quando puro e dissolvido em água, por hidrólise, forma uma solução de caráter....................
O texto é completado de forma correta, respectivamente, por:

etanol - fenol - ácido acético.
ácido acético - etanol - fenol.
ácido acético - fenol - etanol.
fenol - etanol - ácido acético.
fenol - ácido acético - etanol.
Os ácidos carboxílicos e os fenóis, devido ao seu caráter ácido, quando reagem com bases inorgânicas levam à formação de seus respectivos sais orgânicos. Sendo assim, quando ocorrer a reação do ácido pentanóico com o hidróxido de lítio, qual será o sal formado?
Pentanoato de lítio.
Etanoato de potássio.
Propanoato de Lítio.
Hexanoato de Lítio.
Pentanoato de sódio.
A metilamina é um produto gasoso formado na decomposição da carne de peixe, responsável pelo odor característico que impregna as mãos de quem trabalha com peixe. A prática mostra que é mais fácil remover o odor de peixe das mãos esfregando-as primeiro com suco de limão ou vinagre, e depois lavando com água pura, do que diretamente com água e sabão. Com base nestas informações, considere o seguinte texto sobre a metilamina:
A metilamina é um gás bastante solúvel em água. Tem propriedades..............., por conter na molécula o grupo amina. Reage com ................, produzindo o sal CH3NH3+Cl-. Esse sal, quando puro e dissolvido em água, por hidrólise, forma uma solução de caráter....................
O texto é completado de forma correta, respectivamente, por:
Pentanoato de lítio.
Etanoato de potássio.
Propanoato de Lítio.
Hexanoato de Lítio.
Pentanoato de sódio.
A metilamina é um produto gasoso formado na decomposição da carne de peixe, responsável pelo odor característico que impregna as mãos de quem trabalha com peixe. A prática mostra que é mais fácil remover o odor de peixe das mãos esfregando-as primeiro com suco de limão ou vinagre, e depois lavando com água pura, do que diretamente com água e sabão. Com base nestas informações, considere o seguinte texto sobre a metilamina:
A metilamina é um gás bastante solúvel em água. Tem propriedades..............., por conter na molécula o grupo amina. Reage com ................, produzindo o sal CH3NH3+Cl-. Esse sal, quando puro e dissolvido em água, por hidrólise, forma uma solução de caráter....................
O texto é completado de forma correta, respectivamente, por:
A metilamina é um gás bastante solúvel em água. Tem propriedades..............., por conter na molécula o grupo amina. Reage com ................, produzindo o sal CH3NH3+Cl-. Esse sal, quando puro e dissolvido em água, por hidrólise, forma uma solução de caráter....................
O texto é completado de forma correta, respectivamente, por: